Klinik deneyler, bir tıbbi strateji, tedavi veya cihazın insanlar tarafından kullanım veya tüketim için güvenli olup olmadığını belirlemeye yönelik araştırma çalışmalarıdır.
Bu çalışmalar aynı zamanda tıbbi yaklaşımın belirli koşullar veya insanlar için ne kadar etkili olduğunu da değerlendirebilir.
Genel olarak, sağlık bilgisine katkıda bulunur ve sağlık karar verme ve rehberlerine yardımcı olacak güvenilir veriler sağlarlar.
Katılımcının güvenliğini sağlamak için, denemeler küçük gruplar halinde başlar ve yeni bir yöntemin herhangi bir zarara veya tatmin edici olmayan yan etkilere neden olup olmadığını araştırır. Bunun nedeni, bir laboratuarda veya hayvanlarda başarılı olan bir teknik, insanlar için güvenli veya etkili olmayabilir.
Klinik çalışmalarda hızlı gerçekler
- Klinik deneyler, tıbbi bir stratejinin, tedavinin veya cihazın insanlar için kullanımı veya tüketilmesi için güvenli ve etkili olup olmadığını bulmayı amaçlamaktadır.
- Denemeler dört aşamadan oluşur ve bunlar üzerinde odaklanabilir: tedavi, önleme, teşhis, tarama, destekleyici bakım, sağlık hizmetleri araştırması ve temel bilim.
- Bir araştırma ekibi muhtemelen doktorları, hemşireleri, sosyal çalışanları, sağlık profesyonellerini, bilim insanlarını, veri yöneticilerini ve klinik çalışma koordinatörlerini içerecektir.
- Katılım hem riskleri hem de faydaları içerebilir. Katılımcılar, bir araştırmaya katılmadan önce “bilgilendirilmiş onam” belgesini okumalı ve imzalamalıdır.
- Riskler kontrol edilir ve izlenir, ancak tıbbi araştırma çalışmalarının doğası bazı risklerin kaçınılmaz olduğu anlamına gelir.
Klinik deneyler nelerdir?
Klinik çalışmaların temel amacı araştırmadır. Denemeler, hastalıkların veya durumların tedavisi, teşhisi ve önlenmesi ile ilgili tıbbi bilgilere eklenecek şekilde tasarlanmıştır.

Çalışmalar aşağıdakileri amaçlayan katı bilimsel standartları ve yönergeleri takip eder:
- katılımcıları koru
- güvenilir ve doğru sonuçlar sağlamak
İnsanlar üzerinde yapılan klinik deneyler, uzun, sistematik ve kapsamlı bir araştırma sürecinin son aşamalarında ortaya çıkar.
Süreç genellikle yeni konseptlerin geliştirildiği ve test edildiği bir laboratuvarda başlar.
Hayvanların test edilmesi, bilim insanlarının yaklaşımın canlı bir vücudu nasıl etkilediğini görmelerini sağlar.
Son olarak, insan testleri küçük ve daha büyük gruplar halinde gerçekleştirilir.
Denemeler şu şekilde yapılabilir:
- İlaçlar, tıbbi cihazlar veya cerrahi veya terapilere yaklaşımlar gibi bir hastalık, sendrom veya durum için bir veya daha fazla tedavi müdahalesini değerlendirin.
- Örneğin, ilaçlar, aşılar ve yaşam tarzı değişiklikleri yoluyla bir hastalığı veya rahatsızlığı önlemenin yollarını değerlendirin.
- Belirli bir hastalığı veya durumu teşhis edebilecek veya teşhis edebilecek bir veya daha fazla tanı müdahalesini değerlendirin
- Bu durum için bir koşulu veya risk faktörlerini tanımak için tanımlama yöntemlerini inceleyin
- Kronik bir hastalığı olan insanların yaşam kalitesini ve konforunu artırmak için destekleyici bakım prosedürlerini keşfedin
Bir klinik araştırmanın sonucu, yeni bir tıbbi strateji, tedavi veya cihaz olup olmadığını belirleyebilir:
- Hastanın prognozunu olumlu yönde etkiler.
- öngörülemeyen zararlara neden olur
- olumlu yararları yoktur veya olumsuz etkileri vardır
Klinik deneyler, tedavinin maliyet etkinliği, tanı testinin klinik değeri ve tedavinin yaşam kalitesini nasıl iyileştirdiği hakkında değerli bilgiler sağlayabilir.
Klinik deneme türleri
Tüm klinik çalışmaların birincil amacı vardır. Bunlar aşağıdaki kategorilere ayrılabilir:
- Tedavi: Yeni tedavilerin, yeni ilaç kombinasyonlarının veya cerrahi veya terapiye yeni yaklaşımların test edilmesi
- Önleme: Örneğin, ilaçlar, vitaminler, aşılar, mineraller ve yaşam tarzı değişiklikleri yoluyla hastalığın önlenmesini veya nüksetmesini iyileştirmenin yollarını incelemek
- Teşhis: Hastalıkların ve hastalıkların teşhis edilmesi için geliştirilmiş test teknikleri ve prosedürleri bulma
- Tarama: Belli hastalıkları veya sağlık koşullarını tanımlamak için en iyi yöntemi test etmek
- Destekleyici bakım: Kronik hastalığı olan hastalar için yaşam kalitesini ve konforunu artırmak için prosedürleri araştırmak
- Sağlık hizmetleri araştırması: Sağlık hizmetlerinin sunumu, süreci, yönetimi, organizasyonu veya finansmanı hakkında değerlendirme yapılması
- Temel bilim: Bir müdahalenin nasıl çalıştığını incelemek
Klinik çalışmalar neden önemlidir?
Klinik deneyler, tıbbi bakımın iyileştirilmesine ve ilerlemesine yardımcı olur. Çalışmalar hasta bakımını iyileştirmek için kullanılabilecek gerçek kanıtlar sunmaktadır.
Klinik araştırmalar sadece doktorlar aşağıdaki gibi unsurlardan habersizlerse yapılır:
- Yeni bir yaklaşımın insanlarda etkili olup olmadığını ve güvenli olup olmadığını
- Belli hastalıklar ve birey grupları için hangi tedaviler veya stratejiler en başarılı şekilde çalışır?
Klinik çalışmalar nasıl çalışır?
Bir klinik araştırmanın kurulması, yürütülmesi ve takibinde çeşitli unsurlar bulunmaktadır.
Klinik denemeler protokolü

Bir deneme kapsamlı bir plan veya protokol izler. Bir protokol bir klinik araştırmanın yazılı açıklamasıdır.
Çalışmanın amaçlarını, tasarım ve yöntemlerini, ilgili bilimsel geçmişini ve istatistiksel bilgileri içerir.
Dahil edilecek anahtar bilgiler:
- katılımcı sayısı
- kimler katılabilir?
- Hangi testler verilecek ve ne sıklıkla
- toplanacak veri türleri
- çalışmanın uzunluğu
- tedavi planı hakkında detaylı bilgi
Önyargıdan kaçınma
Araştırmacılar önyargıdan kaçınmak için önlem almalıdır.
Önyargı, insan seçimlerini veya protokolle ilgili olmayan ancak araştırmanın sonuçlarını etkileyebilecek diğer faktörleri ifade eder.
Yanlılığı önlemeye yardımcı olabilecek adımlar karşılaştırma grupları, randomizasyon ve maskeleme.
Karşılaştırma grupları
Çoğu klinik çalışma, tıbbi stratejileri ve tedavileri karşılaştırmak için karşılaştırma grupları kullanır. Sonuçlar, bir grubun diğerinden daha iyi bir sonucu olup olmadığını gösterir.
Bu genellikle iki yoldan biriyle gerçekleştirilir:
- Bir grup bir durum için mevcut bir tedaviyi alır ve ikinci grup yeni bir tedavi alır. Araştırmacılar daha sonra hangi grubun daha iyi sonuçlara sahip olduğunu karşılaştırır.
- Bir grup yeni bir tedavi alır ve ikinci grup test ürününe benzeyen bir plasebo, inaktif bir ürün alır.
Rasgeleleştirme
Karşılaştırma gruplarıyla yapılan klinik çalışmalar genellikle randomizasyon kullanır. Katılımcılar, karşılaştırma gruplarına seçimden ziyade şans eseri olarak tahsis edilir. Bu, bir deneme sırasında görülen herhangi bir farklılığın, katılımcılar arasındaki önceden var olan farklılıklardan dolayı değil, kullanılan stratejiden kaynaklanacağı anlamına gelir.
Maskeleme veya kör
Maskeleme veya körleme, katılımcıları veya katılımcıları alacak olan araştırmacıları bilgilendirmeyerek yanlılığı önlemeye yardımcı olur.
Tek kör: Bu, katılımcıların ya da araştırmacıların farkında olmadığı, hangi grubun hangisinin olduğudır.
Çift kör: Bu hem katılımcı hem de araştırmacıların farkında olmadığı zaman.
Şaşırtıcı faktörler
Bir karıştırıcı, iki veya daha fazla özellik arasındaki gerçek ilişkiyi bozabilir.
Örneğin, sigara çakmağı taşıyan kişilerin akciğer kanserine yakalanma olasılığının daha yüksek olduğu, çünkü bir çakmak taşımanın akciğer kanserine neden olduğu sonucuna varılabilir. Sigara içmek bu örnekte bir karmaşadır.
Sigara çakmağı taşıyan kişilerin sigara içmesi daha olasıdır ve sigara içenlerin akciğer kanseri geliştirme olasılığı daha yüksektir, ancak bazı insanlar başka amaçlarla daha hafif bir şekilde taşıyabilirler.
Bunu dikkate almak yanlış sonuçlara yol açabilir.
Araştırma ekibinde kim var?
Genellikle bir tıp doktoru olan bir prensip araştırmacısı, her klinik çalışmayı yönetecektir.
Araştırma ekibi şunları içerebilir:
- doktorlar
- hemşireler
- sosyal çalışanlar
- sağlık profesyonelleri
- Bilim adamları
- veri yöneticileri
- klinik çalışma koordinatörleri
Klinik çalışmalar nerede yürütülmektedir?
Yer, çalışmanın türüne ve kimin organize olduğunu bağlı olacaktır.
Bazı ortak yerler şunlardır:
- hastaneler
- üniversiteler
- tıp merkezleri
- doktor ofisleri
- toplum klinikleri
- federal olarak finanse edilen ve endüstri tarafından finanse edilen araştırma siteleri
Denemeler ne kadar sürer?
Bu, diğer faktörlerin yanı sıra incelenen şeye bağlıdır. Bazı günlerde bazı davalar devam ederken, diğerleri yıllardır devam ediyor.
Bir denemeye kaydolmadan önce, katılımcılara ne kadar sürmesi bekleneceği söylenecektir.
Tasarlanmış ve organizasyon
Farklı çalışma türleri ve bunları organize etmenin farklı yolları vardır. İşte bazı çalışma türleri.
Gözlemsel çalışmalar
Kohort çalışmaları ve vaka kontrol çalışmaları gözlemsel çalışmaların örnekleridir.
Kohort çalışması

Bir kohort çalışması, çalışma popülasyonunun veya kohortun seçildiği gözlemsel bir çalışmadır.
Hangi konuların sahip olduğunu belirlemek için bilgi toplanır:
- söz konusu hastalığın gelişimi ile ilişkili olduğu düşünülen bir kan grubu gibi belirli bir özellik
- Bir hastalığa bağlı olabilecek bir faktöre maruz kalma, örneğin, sigara içimi
Sigara içtikleri için bir birey seçilebilir. Daha sonra, diğer insanlarla karşılaştırıldığında bir hastalık geliştirmenin ne kadar muhtemel olduğunu görmek için zamanında takip edilebilirler.
Bu çalışma, sigara içiminin akciğer kanseri üzerindeki etkisi gibi deneysel olarak kontrol edilemeyen şüpheli risk faktörlerinin etkisini araştırmak için kullanılmıştır.
Kohort çalışmalarının ana avantajları şunlardır:
- Maruziyet hastalık başlangıcından önce ölçülür ve bu nedenle hastalık gelişimi açısından tarafsız olma olasılığı yüksektir.
- Nadir maruziyetler, uygun çalışma kohortları seçimi ile araştırılabilir.
- Birden fazla sonuç – veya hastalık – herhangi bir maruziyet için çalışılabilir.
- Hastalık insidansı hem maruz kalan hem de maruz kalmayan gruplarda hesaplanabilir.
Kohort çalışmalarının ana dezavantajları şunlardır:
- Özellikle ileriye dönük olarak gerçekleştirildikleri takdirde, pahalı ve zaman alıcı olma eğilimindedirler.
- Hem maruziyet durumunda hem de tanı kriterlerindeki zaman içindeki değişiklikler, kişilerin maruziyet ve hastalık durumuna göre sınıflandırılmasını etkileyebilir.
- Sonuç sonuçlarında bilgi yanlılığı olabilir, çünkü öznenin maruz kalma durumu bilinir.
- Takip edilecek kayıplar seçim yanlılığını gösterebilir.
Vaka kontrol çalışmaları
Bir vaka kontrol çalışması, belirli bir tıbbi durum için risk faktörlerini ayırt edebilir.
Araştırmacılar insanları bir durumla ve onsuz olanlarla karşılaştırır. Zamanla geriye doğru çalışarak, iki grubun nasıl farklı olduğunu belirlerler.
Vaka kontrol çalışmaları her zaman geriye dönüktür – geriye dönük – çünkü sonuçla başlarlar ve daha sonra maruziyetleri araştırmak için geri izlerler.
Vaka kontrol çalışmalarının başlıca avantajları şunlardır:
- Bulgular hızlıca elde edilebilir.
- Çalışma en az bir fon veya sponsorluk ile gerçekleşebilir.
- Uzun bir indüksiyon döneminde nadir hastalıkları veya hastalıkları araştırmak için etkilidirler.
- Çok çeşitli olası risk faktörleri incelenebilir.
- Çoklu pozlar çalışılabilir.
- Birkaç çalışma konusu gerektirir.
Vaka kontrollü çalışmaların ana dezavantajları şunlardır:
- İnsidans verileri oluşturulamıyor.
- Önyargılıdırlar.
- Kayıt tutma yetersiz ya da güvenilir değilse, geçmişteki risklerin doğru ve tarafsız ölçülerini almak zor olabilir. Buna bilgi yanlılığı denir.
- Kontrollerin seçimi sorunlu olabilir. Bu, seçim yanlılığını ortaya çıkarabilir.
- Maruziyet ve hastalık arasındaki kronolojik dizinin tanımlanması zor olabilir.
- Maruziyet vakaların büyük bir yüzdesinden sorumlu değilse, nadir maruziyetleri incelemek için uygun değildir.
İç içe vaka kontrol çalışması
Yuvalanmış bir vaka-kontrol çalışmasında gruplar – vakalar ve kontroller – aynı çalışma popülasyonundan veya kohorttan gelir.
Kohort ileri sürüldüğü için, vaka-vaka çalışmasında ortaya çıkan vakalar “vakalar” haline geldi. Kohortun etkilenmemiş katılımcıları “kontroller” haline geldi.
İç içe vaka kontrol çalışmaları, bir kohort çalışmasına kıyasla daha az maliyetli ve daha az zaman alıcıdır.
Hastalığın insidansı ve prevalans oranları zaman zaman iç içe geçmiş bir vaka-kontrol kohort çalışmasından yansıtılabilir. Basit bir vaka kontrol çalışmasından bu mümkün değildir, çünkü toplam maruz kalan kişi sayısı ve takip süreleri genellikle bilinmemektedir.
Yuvalanmış vaka kontrol çalışmalarının başlıca avantajları şunlardır:
- Etkinlik: Kohort katılımcılarının tümü tanısal test gerektirmez.
- Esneklik: Kohort planlandığında tahmin edilmeyen hipotezlerin test edilmesine izin verir.
- Seçim yanlılığının azaltılması: Vakalar ve kontroller aynı popülasyondan örneklenir.
- Bilgi yanlılığının azaltılması: Risk faktörüne maruz kalma, araştırmacı tarafından kör duruma göre değerlendirilebilir.
Ana dezavantaj, sonuçların küçük örnek büyüklüğüne bağlı olarak daha düşük otoriteye sahip olmasıdır.
Ekolojik çalışma
Ekolojik bir çalışma, nüfusun veya topluluğun maruziyeti ile sonucu arasındaki ilişkiye bakar.
Ortak ekolojik çalışma kategorileri şunları içerir:
- coğrafi karşılaştırmalar
- zaman-trend analizi
- göç çalışmaları
Ekolojik çalışmaların başlıca avantajları şunlardır:
- Rutin olarak toplanan sağlık verileri kullanılabildiğinden ucuzdurlar.
- Diğer çalışmalardan daha az zaman alırlar.
- Anlaşılmaz ve anlaşılırlar.
- Gruplar veya alanlar üzerinden ölçülen maruziyetlerin – diyet, hava kirliliği ve sıcaklık gibi – etkileri araştırılabilir.
Ekolojik çalışmaların ana dezavantajları şunlardır:
- Ekolojik yanlışlık olarak bilinen kesinti hataları oluşabilir. Araştırmacılar, bireyler hakkında yalnızca grup verilerinin analizine dayanan sonuçlar çıkardığında olur.
- Sonuç ilişkilerine maruz kalmanın tespit edilmesi zordur.
- Karıştırıcı faktörler hakkında bilgi eksikliği var.
- Pozlamaların nasıl ölçüldüğü alanlar arasında sistematik farklılıklar olabilir.
Deneysel çalışmalar
Gözlemsel çalışmalar dışında, tedavi çalışmaları da dahil olmak üzere deneysel çalışmalar da vardır.
Randomize kontrollü çalışmalar

Randomize kontrollü bir çalışma (RCT), bireyleri belirli bir müdahale almak veya almak için rastgele ayırır.
İki farklı tedaviden biri, ya da bir tedavi ve bir plasebo kullanılacaktır.
Bu, hangi tedavinin en iyi işe yaradığını belirlemek için en etkili çalışma türüdür. Dış değişkenlerin etkisini azaltır.
RCT’lerin başlıca avantajları şunlardır:
- Araştırmacının bilinci veya bilinçaltı yanlılığı yoktur. Bu aslında dış geçerliliği garanti eder.
- Örnek grup yeterince büyük olduğu sürece yaş, cinsiyet, kilo, aktivite düzeyi vb. Gibi değişken değişkenler iptal edilebilir.
RCT’lerin ana dezavantajları şunlardır:
- Zaman alıcılar.
- Pahalı olabilirler.
- Büyük örnek gruplar gerektirirler.
- Nadir olayların incelenmesi zor olabilir.
- Hem yanlış pozitif hem de yanlış negatif istatistiksel hatalar mümkündür.
Uyarlamalı klinik çalışma
Uyarlanabilir bir tasarım metodu toplanan verilere dayanmaktadır. Hem esnek hem de verimli. Deneme ve devam eden klinik çalışmaların istatistiksel prosedürleri için değişiklikler yapılabilir.
Yarı-deney
Yarı deneysel veya “randomize olmayan” çalışmalar, randomize edilmemiş çok çeşitli müdahale çalışmalarını içerir. Bu tür bir deneme, bir RKÇ lojistik olarak mümkün veya etik değilse sıklıkla kullanılır.
Kanıt hiyerarşisi
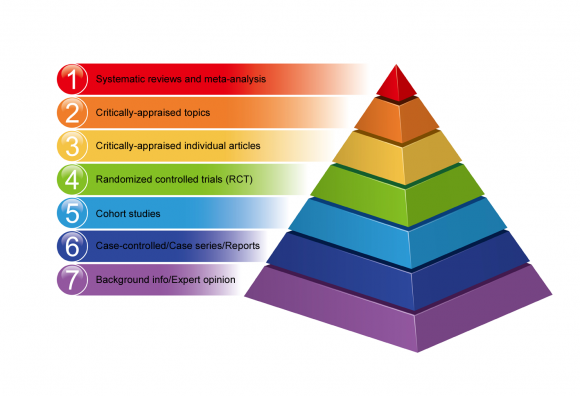
Kanıtların hiyerarşileri, bulgularının geçerliliğine göre çeşitli araştırma yöntemlerinin sıralanmasını mümkün kılmaktadır.
Tüm araştırma tasarımları, sonuçlarında hata ve yanlılık riski açısından eşit değildir. Bazı araştırma yöntemleri, diğerlerinden daha iyi kanıt sağlar.
Aşağıda, altta kanıtların daha düşük bir kalitesinden en üstte yüksek kaliteli kanıtlara kadar uzanan bir piramit formunda kanıta dayalı ilacın hiyerarşisine bir örnek verilmiştir.
Klinik çalışmaların aşamaları
Tıbbi araştırma çalışmaları, faz olarak adlandırılan farklı aşamalara ayrılır. İlaç testi için, bunlar FDA tarafından tanımlanmıştır.
Erken faz denemeleri, bir ilacın güvenliğini ve bunun neden olabileceği yan etkileri araştırır. Daha sonraki denemeler, yeni bir tedavinin mevcut bir tedaviden daha iyi olup olmadığını test eder.
Faz 0 çalışmaları: Farmakodinamik ve farmakokinetik
Faz 0, daha erken bir aşamada yeni bir ilaç için klinik bilgi sağlamaya yardımcı olan bir keşif aşamasıdır.
Bu faz:
- Faz 1’de erken yapılır
- çok sınırlı insan maruziyetini içerir
- Tarama ve mikrodöz çalışmaları ile sınırlı olmak üzere, terapötik veya tanısal bir amacı yoktur.
Faz 1 denemeler: Güvenlik taraması
Evre 0’dan sonra, insanlarda dört faz daha denemesi vardır. Bunlar genellikle üst üste gelir. 1 ile 3 arasındaki aşamalar, bir lisans verilmeden önce gerçekleşir.
Faz 1 yönergeleri şunları içerir:
- 20 ila 80 sağlıklı gönüllü arasında
- ilacın en sık görülen yan etkilerinin doğrulanması
- ilacın metabolize olduğunu ve nasıl atıldığını öğrenmek
Faz 2 denemeleri: Etkinliğin oluşturulması
Faz 1 çalışmaları kabul edilemez toksisite seviyelerini ortaya çıkarmazsa, faz 2 çalışmaları başlayabilir.
Bu içerir:
- 36 ila 300 katılımcı arasında
- ilacın belirli bir hastalık veya rahatsızlığa sahip kişilerde işe yarayıp yaramadığına dair ön veriler toplamak
- Farklı bir ilaç veya plasebo alan benzer bir durumda ilacı alan kişilerle karşılaştırmak için kontrollü çalışmalar
- devam güvenlik değerlendirmesi
- kısa süreli yan etki çalışmaları
Faz 3 çalışmaları: Güvenlik ve etkinliğin nihai teyidi
Eğer faz 2 bir ilacın etkinliğini doğruladıysa, FDA ve sponsorlar 3. aşamada büyük ölçekli çalışmaların nasıl yürütüleceğini tartışacaklardır.
Bu şunları içerecektir:
- 300 ila 3000 katılımcı arasında
- Güvenlik ve etkinlik hakkında daha fazla bilgi toplamak
- farklı popülasyon çalışmaları
- En iyi reçete miktarını belirlemek için çeşitli dozajların incelenmesi
- Etkinliği belirlemek için ilacı diğer ilaçlarla birlikte kullanmak
Bu aşamadan sonra, yeni ilaç hakkında eksiksiz bilgi sağlık yetkililerine sunulur.
Toplantıyı gözden geçir
FDA ürünü pazarlama için onaylarsa, pazarlama sonrası gereksinim ve taahhüt çalışmaları yapılır.
FDA, bu çalışmaları, ürünle ilgili daha fazla güvenlik, etkinlik veya optimal kullanım bilgisi toplamak için kullanır.
Yeni İlaç Uygulaması

Bir ilaç sponsoru, FDA’dan ABD’de pazarlama için yeni bir ilacın onaylanmasını düşünmesini istemek için Yeni Bir İlaç Uygulamasını (NDA) tamamlayacaktır.
Bir NDA şunları içerir:
- tüm hayvan ve insan verileri
- verilerin analizi
- vücutta uyuşturucu davranışları hakkında bilgi
- üretim detayları
FDA’nın gözden geçirilmek üzere kayıt edilip edilmeyeceğine karar vermek için 60 günü vardır.
NDA’yı dosyalamaya karar verirlerse, FDA inceleme ekibi sponsorun uyuşturucu güvenliği ve etkinliği konusundaki araştırmasını değerlendirmek üzere atanır.
Aşağıdaki adımlar daha sonra gerçekleşmelidir.
İlaç etiketleme: FDA, ilacın profesyonel etiketlemesini gözden geçirir ve uygun bilgilerin tüketiciler ve sağlık profesyonelleri ile paylaşıldığını doğrular.
Tesis denetimi: FDA, ilacın üretileceği tesisleri denetler.
Uyuşturucu onayı: FDA hakemleri uygulamayı onaylar ya da bir cevap mektubu verir.
Faz 4 denemeleri: Satışlar sırasında çalışmalar
Faz 4 denemeleri, ilacın pazarlama için onaylanmasından sonra gerçekleşir. Şunları dahil etmek için tasarlanmıştır:
- 1000’den fazla hasta
- Daha geniş bir grupta yeni ilaçların güvenliğini ve etkinliğini ve hastaların alt gruplarını değerlendirmede kapsamlı deneyim
- diğer mevcut tedavilerle karşılaştırma ve kombinasyon
- ilacın uzun süreli yan etkilerinin değerlendirilmesi
- daha az görülen yan etkilerin tespiti
- Diğer geleneksel ve yeni tedavilere kıyasla ilaç tedavisinin maliyet etkinliği
Güvenlik raporu
FDA bir ilacı onayladıktan sonra pazarlama sonrası aşama başlar. Genellikle üretici olan sponsor, FDA’ya periyodik güvenlik güncellemeleri sunar.
Klinik denemelere kim destek veriyor?
Klinik araştırmalar ve araştırmalar yüz milyonlarca dolara mal olabilir. Denemeleri finanse eden gruplar şunları içerebilir:
- ilaç, biyoteknoloji ve tıbbi cihaz şirketleri
- akademik tıp merkezleri
- gönüllü gruplar ve vakıflar
- Ulusal Sağlık Enstitüleri
- Devlet daireleri
- doktorlar ve sağlık sağlayıcıları
- bireyler
Kimler katılabilir?
Protokol, denemeye katılmak için uygun olanları tanımlar.
Muhtemel dahil etme kriterleri şunlar olabilir:
- belirli bir hastalığa veya duruma sahip olmak
- sağlık durumu olmayan “sağlıklı” olmak
Hariç tutma kriterleri, bazı kişilerin bir araştırmaya katılmasını engelleyen faktörlerdir.
Örnekler arasında yaş, cinsiyet, belirli bir hastalık tipi ya da evresi, önceki tedavi öyküsü ve diğer tıbbi durumlar yer alır.
Olası faydalar ve riskler
Klinik çalışmalarda yer almak, katılımcılar için hem fayda hem de risklere sahip olabilir.
Klinik çalışmaların olası faydaları arasında şunlar vardır:
- Katılımcılar yeni tedavilere erişebilir.
- Bir tedavi başarılı olursa, katılımcılar ilk yararlanacaklar arasında olacaktır.
- Yeni bir tedavi alan grupta bulunmayan katılımcılar, belirli bir durum için standart tedaviyi alabilirler, bu da yeni yaklaşımdan iyi veya daha iyi olabilir.
- Sağlık, bir sağlık hizmetleri ekibi tarafından yakından izlenir ve desteklenir.
- Klinik çalışmalardan elde edilen bilgiler bilimsel bilgiye katkıda bulunur, başkalarına yardımcı olabilir ve sonuçta sağlık hizmetlerini geliştirir.
Olası riskler şunlardır:
- Belirli bir durum için standart bakım, bazen, incelenen yeni strateji veya tedavilerden daha iyi olabilir.
- Yeni yaklaşım veya tedavi, bazı katılımcılar için iyi sonuç verebilir, ancak başkaları için zorunlu olmayabilir.
- Özellikle faz 1 ve faz 2 çalışmalarında ve gen terapisi veya yeni biyolojik tedaviler gibi yaklaşımlarda beklenmedik veya öngörülemeyen yan etkiler olabilir.
- Sağlık sigortası ve sağlık sağlayıcıları her zaman klinik çalışmalarda yer alan hastalara hasta bakımını ve masraflarını kapsamaz.
Rıza vermek ne anlama geliyor?

Bilgilendirilmiş onam belgesi, klinik araştırmaya katılmanın risklerini ve potansiyel faydalarını açıklar.
Belgedeki görünmesi gereken öğeler arasında şunlar bulunur:
- araştırmanın amacı
- öngörülebilir riskler
- olası faydalar
Katılımcılardan onay belgesini iyice okuması, araştırmaya dahil edilmeden önce kayıt ve imzalamak isteyip istemediğine karar vermesi beklenir.
Klinik çalışmalar güvenli midir?
FDA, bir araştırmaya katılmayı düşünen herkesin, riskler hakkında bilgiler de dahil olmak üzere, bilinçli bir seçim yapmak için ihtiyaç duydukları tüm güvenilir bilgilere erişebilmesini sağlamak için çalışır.
Katılımcılara yönelik riskler kontrol edilir ve izlenirken, tıbbi araştırma çalışmalarının doğası gereği bazı riskler kaçınılmaz olabilir.
Katılımcılar nasıl korunur?

Katılımcıların güvenliği yüksek öncelikli bir konudur. Her denemede, bilimsel gözetim ve hasta hakları onların korunmasına katkıda bulunur.
İyi klinik uygulama (GCP), denemelerde etik ve uygun prosedürlerin takip edilmesini sağlamayı amaçlamaktadır.
GCP uyumu, halkın, katılımcıların güvenlik ve haklarının korunduğundan emin olmasını sağlar.
Amaç:
- Katılımcıların haklarını, güvenliğini ve refahını korumak
- Toplanan verilerin güvenilir olduğunu, bütünlüğünü ve uygun kalitede olduğunu garanti etmek
- klinik araştırmanın yürütülmesi için kurallar ve standartlar sağlamak
GCP’nin temelleri ilk olarak 1947’de ortaya konmuştur. Başlıca noktalar, herhangi bir denemede araştırmacıların şunları garanti etmesidir:
- gönüllü katılım
- bilgilendirilmiş onam
- riskin minimize edilmesi
Zaman içinde, eklemeler, savunmasız popülasyonlar için, araştırma yürüten kuruluşlara rehberlik sağlamak için ek koruma oluşturmaya kadar değişmiştir.
Hasta hakları
Hasta haklarını koruma yolları şunlardır:
Bilgilendirilmiş onam, klinik deneme katılımcılarına araştırmayla ilgili tüm gerçekleri sağlama sürecidir. Katılımcılar, araştırmaya katılmayı kabul etmeden önce olur. Bilgilendirilmiş onam, alınabilecek tedaviler ve testler ile olası fayda ve riskler hakkında detayları içerir.
Diğer haklar: Bilgilendirilmiş izin belgesi bir sözleşme değildir; Katılımcılar, araştırmanın tamamlanmış olup olmadığına bakılmaksızın, herhangi bir zamanda araştırmayı geri çekebilir.
Çocuklar için haklar ve korunma: Bir çocuk veya yasal vasi, çocuğun 18 yaşında veya daha küçük olması durumunda yasal onay vermelidir. Bir denemenin asgari düzeyde bir risk içermesi durumunda, her iki ebeveyn de izin vermelidir. 7 yaşın üzerindeki çocuklar klinik çalışmalarda yer almayı kabul etmelidir.
Bir klinik araştırmayı nasıl bulabilirim?
Güncel klinik denemeler hakkında bilgi burada bulunabilir.